L'eau, à la source de la vie
En cette Journée internationale de l'eau, notre scientifique embarquée, Dr Katia Nicolet, se jette à l'eau pour découvrir cette molécule aussi merveilleuse que magique qui occupe une place cruciale dans nos vies. Une importance que nous avons tendance à oublier. Découvrez-en plus sur les pouvoirs de l'eau, et vous ne verrez plus jamais un verre d'eau de la même façon.

Plongée sous les sargasses
La molécule de vie
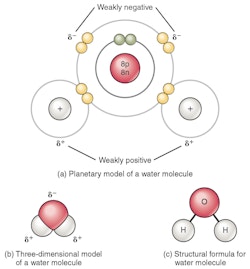
La molécule d'eau possède des propriétés uniques qui permettent la vie sur terre - ou plutôt, la vie a évolué grâce aux qualités particulières de l'eau. Autrement dit, l'eau est synonyme de vie sur notre planète bleue. Celle-ci est composée d'un atome d'oxygène (O) et de deux atomes d'hydrogène (H). Ensemble, ils forment une molécule globalement stable et électriquement neutre (celle-ci n'étant pas chargée). Toutefois, les électrons préférant être plus proches de l'atome d'oxygène que des atomes d'hydrogène, la molécule finit par avoir une configuration en Y : cela signifie que les deux atomes d'hydrogène sont plus proches l'un de l'autre d'un côté.
Par conséquent, un côté de la molécule est légèrement chargé positivement, tandis que l'autre est légèrement chargé négativement. Cette polarité (légère charge positive/négative) permet à la molécule de se comporter comme un aimant en étant "attirée" par d'autres molécules d'eau ou d'autres molécules polarisées. La faible liaison entre l'hydrogène d'une molécule d'eau et l'oxygène d'une autre molécule d'eau s'appelle une liaison hydrogène, et elle rend l'eau presque magique.
Grâce à sa polarité, l'eau est un puissant solvant ! Si l'on prend la molécule de sel (NaCl) par exemple, celle-ci est séparée par l'eau, car le Na+ est attiré par O2- et le CL- par H+. Le sel est donc dissous dans l'eau, ce qui explique la salinité de nos océans. C'est également de cette manière que l'eau peut dissoudre les minéraux dans les roches et les sédiments, lui permettant de devenir une source importante de minéraux pour les humains, les animaux et les plantes. 20 % de notre apport quotidien en calcium et en magnésium, par exemple, provient de l'eau potable (Olivares M. & Uauy R., 2005, Essential nutrients in drinking water, Organisation Mondiale de la Santé).
Glace flottante : pas de panique ?
Les liaisons hydrogène entre les molécules d'eau donnent lieu à une autre propriété appelée cohésion. Celle-ci signifie que les molécules d'eau se collent les unes aux autres, ce qui, à son tour, permet la capillarité. C'est face à cette capillarité que l'eau circule dans les tissus végétaux et les vaisseaux sanguins, même contre la force de gravité. Magique. Ou physique, à vous de décider. La cohésion est également responsable de la tension superficielle, ce qui explique que l'eau peut former un dôme à la surface d'un verre légèrement trop rempli, ou que les stridents (insectes) peuvent marcher sur l'eau sans en briser la surface.
Le plus absurde étant que cette adhérence supplémentaire signifie qu'à température ambiante, l'eau est liquide plutôt que gazeuse, grâce aux liaisons hydrogène ! Bien que les liaisons hydrogène se forment et se brisent continuellement lorsque les molécules d'eau se déplacent, l'adhérence est suffisante pour maintenir les molécules d'eau proches les unes des autres et l'empêcher d'être un gaz à 20°C. De plus, les liaisons dans l'eau liquide maintiennent les molécules très proches les unes des autres, mais lorsque l'eau gèle, les molécules s'arrangent en un cristal, créant plus d'espaces entre celles-ci. C'est pourquoi l'eau liquide est plus dense que l'eau solide.

Glacier au Spitzberg
Ceci est extrêmement important. Nous avons toujours connu la glace flottant sur l'eau, nous ne nous sommes donc jamais questionnés face à ce phénomène. Mais pouvez-vous songer à un autre élément qui est plus dense sous forme liquide que solide ? Le plomb solide flotte-t-il sur le plomb liquide ? L'huile solide (la graisse) flotte-t-elle sur l'huile liquide ? Non, car l'état liquide signifie généralement que les molécules sont plus exaltées, qu'elles bougent davantage et qu'il y a donc plus d'espace entre elles. Mais pas l'eau. L'eau la plus dense est en fait à une température de 4°C, et la moins dense -vous l'aurez sans doute deviné- à 0°C. D'autant plus magique.
Vie et mort dues à la glace
La glace occupe donc plus d'espace que l'eau. Vous en avez probablement fait l'expérience lorsque la bouteille d'eau que vous avez laissée dans le congélateur a explosé, ou lorsqu'une conduite d'eau a éclaté au cours de l'hiver. Cette propriété de la glace a des conséquences importantes sur l'altération de la matière et la création de sédiments par érosion. C'est également la raison pour laquelle la plupart des organismes meurent lorsqu'ils gèlent, car la formation de glace à l'intérieur des cellules transperce la membrane cellulaire. Seuls quelques animaux et plantes possédant des protéines antigel peuvent survivre à la chute de leur température corporelle sous 0°C. C'est pourquoi, si vous étiez cryogénisé, vous vous transformeriez en une flaque de sang et de tissus une fois décongelés. À moins que vous ne soyez un poisson cool de l'Antarctique.
Une glace moins dense est aussi synonyme de vie. Si l'eau solide était plus dense que l'eau liquide, les lacs, les rivières et les océans gèleraient de bas en haut. Dès que des cristaux de glace se formeraient, ils couleraient et s'accumuleraient au fond, jusqu'à ce que tout gèle. Toute la diversité des bactéries, des plantes, des invertébrés, des poissons et des amphibiens qui vivent dans les lacs et dans les océans polaires mourrait chaque année, ce qui aurait un impact considérable sur la biodiversité aquatique. Au lieu de cela, la glace se forme à la surface, ajoutant une couche modérément froide (0°C) entre l'eau et les conditions souvent plus fraiches de l'environnement. Les organismes aquatiques sont ainsi à l'abri des températures glaciales et peuvent survivre jusqu'au printemps.
La planète bleue

Plongée sous les sargasses
Il est évident que l'eau est une molécule singulière dont la vie sur Terre dépend, la planète étant recouverte à 70% par des océans ! Cependant, en tant qu'organismes non marins, l'eau salée n'est pas potable. Si nous devions boire de l'eau salée, l'eau contenue dans nos cellules tenterait de dissoudre l'eau salée par un processus appelé osmose, et nous finirions par gravement nous déshydrater. Il en va de même pour les plantes et les animaux non marins. Par conséquent, les organismes terrestres et d'eau douce dépendent de l'eau douce. Or, il y a étonnamment peu d'eau douce sur terre !
De toute l'eau présente sur terre, 97,5% sont de l'eau salée ! Il reste donc un modeste 2,5 % d'eau douce sur cette planète (environ 34 650 000 km3). Mais attendez ! Sur l'ensemble de l'eau douce, environ 69 % sont stockés dans les glaciers, les calottes glaciaires et les sols gelés (permafrost ; les chiffres sont arrondis). Ainsi, seulement 31% de l'eau douce sur terre est réellement disponible pour la vie, dont la grande majorité (30%) est constituée d'eaux souterraines, et seulement 1% de toute l'eau douce du monde est constituée d'eaux de surface (435 100 km3).

L’importance de l'eau des sols
Les eaux souterraines constituent toutes les eaux qui s'infiltrent et percolent dans le sol pour atteindre les aquifères souterrains. Ceux-ci sont constitués de différents matériaux (sable, graviers, roches sédimentaires perméables, roches volcaniques et cristallines) qui retiennent l'eau des précipitations de surface et de la fonte des neiges. Même si l'eau de surface est ce que nous pouvons voir et expérimenter tous les jours, les eaux souterraines fournissent la majeure partie de l'eau que la population mondiale utilise (agriculture, élevage, industrie) et boit. Dans certaines régions arides, c'est la seule source d'eau douce disponible. Ainsi, 2,5 milliards de personnes dépendent uniquement des eaux souterraines comme source d'eau quotidienne.
Ce stockage d'eau souterraine est également extrêmement important pour les habitats et la végétation vivants à la surface. Il joue un rôle clé dans le maintien du niveau et du débit de l'eau dans les rivières, les lacs et les zones humides, en particulier pendant les mois les plus secs. Ce flux d'eau à travers le sol est essentiel pour la faune et la végétation, seules les plantes résistantes à la dessiccation pouvant vivre sur des zones éloignées des eaux souterraines (certaines régions élevées).
Consommation et pollution des eaux souterraines
Nos besoins en eau sont difficiles à appréhender. Ceci étant dit, afin de vous donner une idée, le régime alimentaire d'un Américain moyen, par la culture et l'élevage, nécessite 5 000 litres d'eau par jour ! À l'échelle mondiale, l'irrigation représente plus de 70 % du prélèvement total d'eau, qu'il s'agisse d'eau de surface ou d'eau souterraine. Environ 45% de l'utilisation totale de l'eau d'irrigation provient des eaux souterraines. Et cela ne concerne que les besoins de la population humaine. Les animaux et les écosystèmes ont eux aussi besoin de grandes quantités d'eau douce pour maintenir la biodiversité et la vie. Les écosystèmes d'eau douce abritent une grande variété de plans et d'animaux, et ces écosystèmes connaissent actuellement un taux d'extinction jusqu'à 15 fois supérieur à celui des écosystèmes marins ! Pour toutes ces raisons, l'eau douce est immensément importante.

Spitzberg
Malheureusement, les systèmes d'eau douce, et les eaux souterraines en particulier, sont menacés par la surconsommation, la dégradation et la pollution. Des puits ont vidé des aquifères entiers là où les besoins en eau de la population humaine dépassaient l'apport d'eau provenant des précipitations. L'abaissement du niveau de certains aquifères proches de l'océan entraîne parfois des infiltrations d'eau salée dans le sol poreux, rendant l'eau souterraine imbuvable et inutilisable pour les cultures. Enfin, toutes sortes de polluants d'origine humaine peuvent s'infiltrer dans le sol avec les précipitations et contaminer les réservoirs d'eau souterraine. Une liste non exhaustive comprend les pesticides et les engrais provenant des champs, les sels provenant des routes, les produits chimiques provenant des décharges, la pollution organique provenant des fosses septiques et des systèmes d'égouts non étanches, etc.
Pour une meilleure gestion de l'eau
L'eau douce est une ressource limitée sur notre planète et nous, ainsi que des centaines de milliers d'espèces, en dépendons pour notre survie. Avec l'aggravation du changement climatique, les eaux souterraines vont devenir encore plus critiques. Nous avons besoin d'une gestion plus durable des systèmes d'eaux souterraines dans le monde entier. En cette Journée internationale de l'eau, nous devons "rendre visible l'invisible" et veiller à ce que les eaux souterraines, bien que cachées, ne le soient pas de nos esprits.